Es un gusto presentar el nuevo documento intersocietario sobre Apolipoproteína B (ApoB), que resalta la importancia clínica de su medición en la evaluación del riesgo cardiovascular.
Esta actualización, fruto del trabajo conjunto de distintas sociedades científicas y profesionales, entre las que participó la FBA, ofrece recomendaciones prácticas y revisa la evidencia actual que respalda el uso de apoB como marcador más preciso que el colesterol LDL (C-LDL) en determinadas situaciones clínicas. También se discute la correlación y la concordancia entre la apoB, el C-noHDL y el C-LDL.
Invitamos a todos los profesionales a consultar este material clave para la práctica bioquímica actual.
Información sobre el tema
¿Qué es la apolipoproteína B ?
La Apolipoproteína B (ApoB) es el principal componente proteico de las partículas lipoproteicas aterogénicas, como las de muy baja densidad (VLDL), densidad intermedia (IDL) y baja densidad (LDL). Por lo tanto, la concentración plasmática de ApoB permite estimar el número total de partículas aterogénicas. En los últimos años, diversos estudios epidemiológicos y de intervención han demostrado que la medición de ApoB predice de forma independiente el riesgo cardiovascular, incluso superando a los parámetros lipídicos convencionales, como el colesterol unido a la LDL (C-LDL), que continúa siendo el principal objetivo terapéutico en el tratamiento lipídico, con metas claramente establecidas. 1
¿Cuáles son los objetivos de este trabajo ?
El objetivo de este trabajo colaborativo entre prestigiosas sociedades científicas es desarrollar un documento de posición que aborde, de manera clara y práctica, diversos aspectos relacionados con la medición de la ApoB, mediante la respuesta a diez preguntas clave. Los principales mensajes se resumen en la figura central.
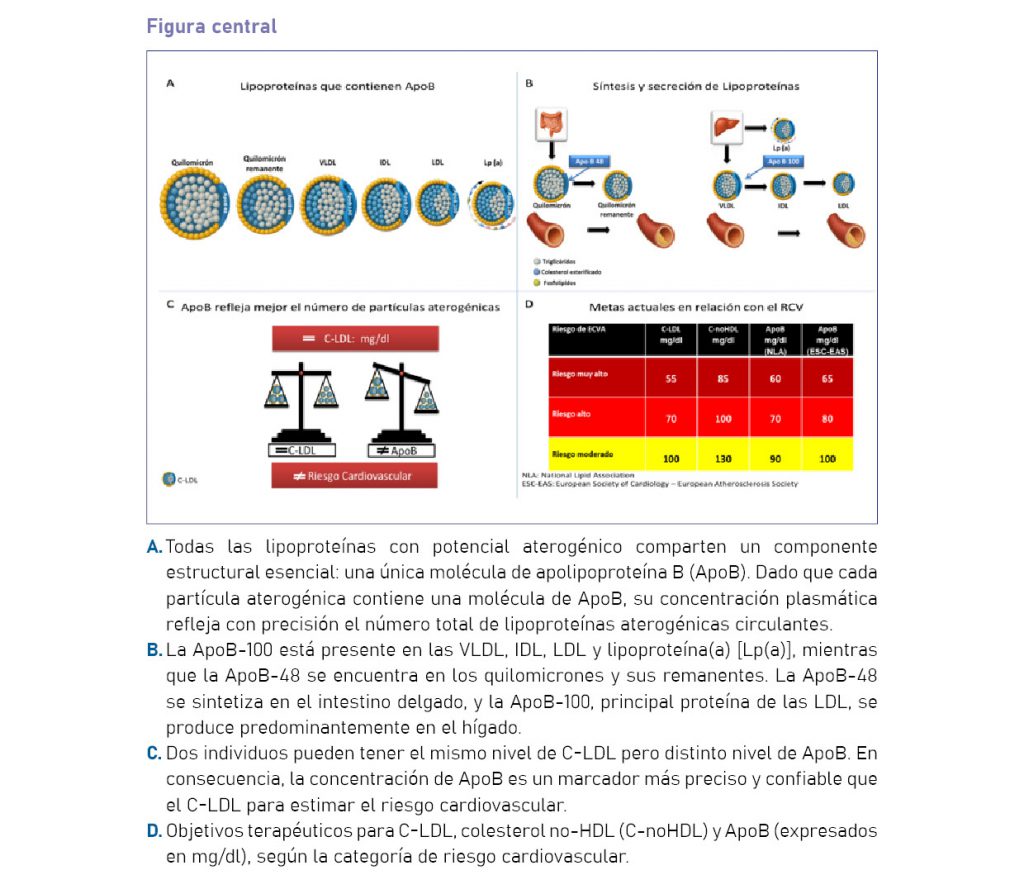
¿Qué debemos conocer sobre la fisiología de la ApoB?
Todas las lipoproteínas con potencial aterogénico contienen una ApoB como componente estructural principal, la cual no es intercambiable. En contraste, las lipoproteínas de alta densidad (HDL), reconocidas por sus propiedades antiaterogénicas, integran en su membrana la apolipoproteína A-I (ApoA).
La ApoB-100 se encuentra intrínsecamente asociada a las VLDL, sus remanentes (IDL), las LDL, así como la ApoB-48 a los quilomicrones y sus remanentes. Dado que cada una de estas partículas contiene una única molécula de ApoB, la concentración plasmática total de ApoB refleja con precisión el número total de partículas lipoproteicas aterogénicas circulantes en la sangre. 2
El gen que codifica la ApoB se localiza en el brazo corto del cromosoma 2 y consta de 29 exones. Este gen da lugar a dos isoformas: la ApoB-100, que contiene 4536 aminoácidos (550 kDa), y la ApoB-48 (265 kDa), que es una versión truncada de la primera, con aproximadamente la mitad de su longitud. La formación de ApoB-48 ocurre en el intestino delgado mediante un proceso único de edición del ARN mensajero (ARNm): una desaminación postranscripcional altamente específica de la citidina, mediada por una enzima de edición del ARNm llamada APOBEC-1. 3 La ApoB-100 se sintetiza principalmente en el hígado y es el principal determinante proteico de las LDL, siendo reconocida por el receptor apoB/E (receptor de LDL). Este reconocimiento activa el catabolismo de las LDL, mediado por dicho receptor.4
Finalmente, aunque menos frecuentes que las mutaciones en el receptor de LDL, las mutaciones en el gen APOB pueden provocar hipercolesterolemia familiar.3
La insulina desempeña un papel central en la coordinación del metabolismo de las lipoproteínas. Los altos niveles de insulina actúan sobre el adipocito para promover la captación de triglicéridos activando la lipoproteína lipasa (LPL) e inhibir la liberación de ácidos grasos libres por intermedio de la inhibición de la lipasa hormono sensible. Esto promueve el almacenamiento de triglicéridos para su uso posterior. En ayunas, este proceso se invierte: los niveles de insulina disminuyen y los ácidos grasos libres se liberan del adipocito y se entregan al hígado. El hígado reesterifica los ácidos grasos a triglicéridos y los secreta como VLDL. Además, la capacidad del tejido adiposo para captar triglicéridos se ve afectada en ausencia de insulina y, por lo tanto, los triglicéridos son utilizados preferentemente por otros tejidos, como el músculo esquelético y el hígado.5
La síntesis y secreción de la ApoB es un proceso altamente complejo. Sorprendentemente, la mayor parte de la ApoB sintetizada es degradada antes de ser secretada, por lo que la cantidad final de ApoB liberada al medio extracelular depende en gran medida de la proporción del polipéptido recién sintetizado que logra escapar a los mecanismos de degradación intracelular. La insulina regula la secreción de ApoB a través de múltiples mecanismos, actuando en tres niveles principales:
1) Disminuye la síntesis de la proteína microsomal transportadora de triglicéridos (MTP), esencial para el ensamblaje de las lipoproteínas de muy baja densidad (VLDL);
2)estimula la degradación de ApoB mediante el sistema ubiquitina-proteasoma, responsable de su eliminación intracelular;
3) Favorece la degradación de ApoB a través del sistema fagolisosomal, otro mecanismo de degradación celular. 5-6
¿Cuáles son los métodos disponibles para su cuantificación?
Medir un componente lipídico, como el colesterol de las lipoproteínas, puede resultar más práctico y ligeramente más económico. Sin embargo, debido a la variabilidad en el contenido de colesterol entre las partículas de cada familia lipoproteica, la estandarización de los métodos para cuantificar el C-LDL o el colesterol unido a las HDL (C-HDL) resulta más compleja que la medición selectiva de una molécula proteica definida y estructuralmente constante, como la ApoB.7 Además, la ApoB se comporta como un marcador robusto, ya que puede medirse de forma precisa en todo el rango de concentraciones, tanto en condiciones normales como patológicas, sin verse afectada por las posibles variaciones fisiopatológicas.
Los métodos utilizados por los laboratorios clínicos para la medición de ApoB son completamente automatizables y se basan en técnicas de inmunoturbidimetría o inmunonefelometría. Estos deben cumplir con los estándares establecidos por la Organización Mundial de la Salud (OMS) y la Federación Internacional de Química Clínica (IFCC, de su siglas en inglés), mediante el uso de calibradores trazables a materiales de referencia internacionales, actualmente el SP3.8 Ambos métodos utilizan anticuerpos específicos contra ApoB.
El fundamento de la inmunoturbidimetría se basa en la formación de inmunocomplejos con el anticuerpo dirigido contra la ApoB a medir. Luego se mide la difracción de la luz en un ángulo determinado la cual se altera por los inmunocomplejos formados. En el caso de la inmunonefelometría, puede ser de “punto final” cuando se mide la difracción de la luz en un ángulo determinado, alterada por los inmunocomplejos formados, o “cinética” cuando se mide el cambio de la velocidad de emisión de la luz dispersada, en función de la velocidad de formación de los inmunocomplejos.
El equipamiento necesario para medir ApoB, así como las especificaciones de calidad y experiencia requeridas, están disponibles en una gran cantidad de laboratorios clínicos. Además, varias empresas de diagnóstico fabrican los ensayos aprobados para su medición. Los métodos estándar mencionados son equivalentes a otros procedimientos validados y robustos, como la resonancia magnética nuclear, cuyo equipamiento está destinado a laboratorios especializados y que también se utiliza para analizar subfracciones lipoproteicas.9 Desde la década de 1990, la IFCC ha impulsado la estandarización de la medición de ApoB, estableciendo un método de referencia provisional basado en la medida, por inmunonefelometría, de la proteína total de LDL previamente aislada por ultracentrifugación. En los últimos años, la IFCC ha comenzado a evaluar la cromatografía líquida-espectrometría de masas en tándem (LC-MS/MS) como candidato a método de referencia definitivo, lo cual permitirá una verdadera estandarización de la medición de ApoB, transformándola en el primer marcador de lipoproteínas verdaderamente estandarizado.7,10 Por el momento, diversos grupos de consenso, organizadores de la Evaluación Externa de Calidad, el Programa de Estandarización de Lípidos del Centro para el Control y la Prevención de Enfermedades de EEUU (CDC, por sus siglas en inglés) y otros expertos en química clínica, han confirmado que el programa de estandarización de ApoB desarrollado por la OMS/IFCC cumple con los requisitos necesarios para su aplicación en la atención clínica. 10 Todos los métodos miden ApoB total (ApoB100+ApoB48), sin embargo el aporte postprandial de ApoB48 en relación con ApoB100 es mínimo e insignificante, salvo cuando los triglicéridos superan los 400 mg/dl, por lo que la ApoB puede medirse sin necesidad de ayuno en la mayoría de los casos. Las muestras de suero pueden ser congeladas y luego descongeladas para su medición. 10
¿Qué relación existe entre la ApoB y el riesgo cardiovascular según los estudios epidemiológicos y de aleatorización mendeliana?
A partir de lo previamente comentado, es razonable plantear que niveles elevados de ApoB se asocian con un mayor riesgo cardiovascular. Sin embargo, aunque esta idea parece lógica desde el sentido común, es necesario respaldarla con evidencia científica.
La evidencia proveniente de estudios poblacionales demuestra que niveles elevados de ApoB se asocian con un incremento en el riesgo de desarrollar eventos cardiovasculares. Johannesen y col. realizaron un análisis del Copenhagen General Population Study en el que incluyeron 53484 mujeres y 41624 hombres que no recibían estatinas y evaluaron la relación entre los niveles elevados de ApoB y la incidencia de eventos cardiovasculares.11 Luego de una mediana de seguimiento de 9,6 años evidenciaron una asociación concentración-dependiente entre los niveles elevados de ApoB y el riesgo de presentar un infarto agudo de miocardio y enfermedad cardiovascular aterosclerótica. Este trabajo demostró que la ApoB presenta un valor predictivo importante más allá del C-LDL en todo el espectro de concentración de esta lipoproteína tanto en hombres como en mujeres. Antes de este estudio, Sniderman y col. publicaron un metaanálisis de estudios observacionales que incluyó a 233455 pacientes, en el cual demostraron que la ApoB es un mejor predictor del riesgo cardiovascular que el C-LDL y el C-noHDL.12 La razón de riesgo relativa para ApoB fue de 1,43 [Intervalo de confianza (IC) 95%: 1,35–1,51], en comparación con 1,25 para el C-LDL (IC 95%: 1,18–1,33) y 1,34 para el C-noHDL [IC 95% 1,24-1,44).
En la misma línea, estudios de aleatorización mendeliana han evidenciado que las personas portadoras de variantes genéticas asociadas a niveles elevados de ApoB presentan un mayor riesgo de desarrollar eventos cardiovasculares en comparación con quienes no las poseen. En particular, un análisis del UK Biobank mostró que la ApoB se asoció, en un análisis multivariado, con casi el doble de riesgo de enfermedad cardiovascular [Odds Ratio (OR): 1,92; IC 95%: 1,31–2,81; p<0,001].13 Por otro lado, otro estudio de aleatorización mendeliana demostró que en casos de discordancia entre los niveles de C-LDL y ApoB, esta última se correlaciona de manera más precisa con el riesgo cardiovascular. 14
¿Cuál es la asociación entre los niveles de ApoB durante el tratamiento y el riesgo cardiovascular según los ensayos clínicos?
Dado que la mayoría de los estudios clínicos controlados y aleatorizados incluyeron pacientes en función del riesgo cardiovascular y de los niveles de C-LDL, la evidencia disponible específicamente sobre ApoB es más limitada. Además, estos ensayos generalmente evaluaron esquemas terapéuticos sin establecer objetivos específicos de ApoB como meta de tratamiento. No obstante, el análisis de muchos de estos estudios revela una correlación directa entre los niveles de ApoB alcanzados durante el tratamiento y la incidencia futura de eventos cardiovasculares mayores.
Múltiples ensayos clínicos con estatinas han demostrado que el valor intratratamiento de ApoB posee un valor predictivo independiente en relación con los eventos cardiovasculares mayores. Estos hallazgos se han observado tanto en contextos de prevención primaria15 como secundaria.16 Un metanálisis que incluyó siete estudios clínicos aleatorizados con estatinas mostró que la reducción media del riesgo de cardiopatía coronaria por cada disminución de una desviación estándar (27 mg/dl) en los niveles de ApoB fue del 24,4%, lo que representó una reducción de riesgo mayor en comparación con el C-LDL (20,1%) o el C-noHDL (20%). 17 En este análisis, la concentración media de ApoB al año en el grupo tratado fue de 85 mg/dl, con un rango de valores entre 71 y 104 mg/dl.
En el estudio IMPROVE-IT, la adición de ezetimibe a simvastatina, en comparación con simvastatina sola, en pacientes con síndrome coronario agudo, se asoció con una reducción del 15% en los niveles de ApoB (mediana intratratamiento de 67 mg/dl) y con una disminución del 6,4% en la incidencia de eventos cardiovasculares combinados a los 6 años de seguimiento.18 Tanto en este estudio como en FOURIER, que evaluó el efecto de evolocumab frente a placebo en pacientes en prevención secundaria tratados con estatinas, el nivel de ApoB alcanzado durante el tratamiento fue el mejor predictor de infarto de miocardio. 19 De manera similar, en el ensayo ODYSSEY OUTCOMES, que investigó el impacto de alirocumab en 18000 pacientes con síndrome coronario agudo frente a placebo, se observó que un mayor nivel basal de ApoB se asociaba con una mayor tasa de eventos cardiovasculares combinados, así como con una mayor reducción relativa y absoluta de eventos en el grupo tratado con alirocumab. 20
Además, niveles bajos de ApoB durante el tratamiento (<35 mg/dl) fueron altamente predictivos de una mayor reducción de eventos clínicos. En cuanto a los niveles intratratamiento de ApoB, se reportaron valores de 38 mg/dl en FOURIER y de 49 mg/dl en ODYSSEY OUTCOMES, lo cual se asoció con una reducción del 15% en los eventos cardiovasculares combinados en ambos estudios, con seguimientos de 2,2 y 2,8 años, respectivamente. En el estudio REVEAL, que evaluó el inhibidor de CETP anacetrapib frente a placebo en pacientes en prevención secundaria tratados con estatinas, una reducción de ApoB de 12 mg/dl (18%) se asoció con una disminución del 9% en la incidencia de eventos cardiovasculares.21 De forma similar, en el ensayo REDUCE-IT, que utilizó ácido eicosapentaenoico (EPA) purificado, una reducción del 10% en los niveles de ApoB se asoció con una disminución del 25% en los eventos cardiovasculares.22 Por el contrario, en el estudio STRENGTH, que empleó una combinación de EPA y ácido docosahexaenoico (DHA), no se observó una reducción significativa de ApoB ni de eventos cardiovasculares, lo que refuerza la coherencia de la asociación entre el descenso de ApoB y la disminución del riesgo cardiovascular. 23
Un metaanálisis que incluyó 29 estudios clínicos con un total de 332912 pacientes evaluó si la reducción de eventos cardiovasculares asociada al descenso de ApoB dependía del tipo de fármaco utilizado. 24 Aunque la magnitud de la reducción de eventos fue mayor en los estudios con estatinas, estos ensayos tuvieron un seguimiento medio ponderado más prolongado en comparación con aquellos realizados con otros tratamientos, como los inhibidores de PCSK9. Un análisis comparativo entre los estudios FOURIER y SPIRE, que emplearon anticuerpos monoclonales inhibidores de PCSK9, y el metaanálisis del grupo CTT (Cholesterol Treatment Trialists’ Collaboration), que incluyó los principales ensayos con estatinas, concluyó que la reducción de eventos cardiovasculares observada con los inhibidores de PCSK9 fue coherente con la esperada durante los primeros dos años de tratamiento con estatinas. 25
En resumen, la evidencia disponible es consistente en demostrar que, independientemente del fármaco utilizado, la reducción de ApoB per se se asocia con una disminución significativa del riesgo de eventos cardiovasculares futuros. Aunque los resultados de los ensayos clínicos pueden variar según el tiempo de exposición al tratamiento, el contexto clínico del paciente y las características de la población incluida, la evidencia respalda de manera robusta que la reducción de ApoB durante el tratamiento constituye un objetivo terapéutico central, asociado de forma consistente con la disminución del riesgo de eventos cardiovasculares.
¿Cuál es la correlación y la concordancia entre la ApoB, el C-noHDL y el C-LDL?
Los conceptos de concordancia y correlación son ampliamente utilizados para evaluar la asociación entre variables, pero, aunque están relacionados, representan enfoques distintos. 26 La correlación se enfoca en la relación entre los cambios observados en dos variables, es decir, cómo varía una en función de la otra. En cambio, la concordancia se centra en el grado de coincidencia entre dos métodos de medición o clasificación de una misma variable. Así, mientras la correlación mide asociación, la concordancia evalúa el grado de acuerdo entre los resultados.
Numerosos estudios han analizado la correlación y la concordancia entre distintos marcadores lipídicos. Un estudio analizó los perfiles lipídicos de participantes sin enfermedades cardiovasculares pertenecientes al UK Biobank (n = 308182), al Women’s Health Study (n = 26204) y al Framingham Heart Study (n = 2839).27 El análisis evidenció una buena correlación entre los distintos marcadores lipídicos. En particular, la correlación entre ApoB y C-LDL mostró valores de “r” entre 0,80 y 0,96, mientras que la correlación entre ApoB y el C-noHDL presentó valores de “r” entre 0,85 y 0,96.
Está bien establecido que existe discordancia entre el C-LDL y el C-noHDL para un mismo valor de ApoB.28 Un análisis post hoc de los datos de InPractice, que incluyó pacientes con enfermedad cardiovascular tratados con diferentes esquemas hipolipemiantes, mostró que la concordancia entre ApoB y C-noHDL osciló entre el 60,6% y el 62,4%. Además, el análisis kappa confirmó una concordancia moderada entre los niveles de C-LDL y ApoB en todos los grupos de tratamiento, con valores que variaron entre 0,54 y 0,59. 29
Datos del Reino Unido indican que, a pesar de las altas correlaciones de entre ApoB y C-noHDL (≥ 0,95) a nivel poblacional —y una correlación ligeramente menor entre ApoB y C-LDL—, existe una amplia variabilidad en la concentración de ApoB para un valor dado de C-noHDL o C-LDL.30 Asimismo, utilizando los percentiles poblacionales de C-LDL, C-no-HDL y ApoB de adultos no tratados en la Encuesta Nacional de Salud y Nutrición (NHANES) 2005–2016, para un valor de C-noHDL de 100 mg/dl (aproximadamente en el percentil 10–20 de la población), el rango de valores de ApoB fue de 52 a 78 mg/dl (aproximadamente del percentil 5 al 30).30 De forma similar, para un valor de C-no-HDL de 160 mg/dl (percentil 70–80), los valores de ApoB se situaron entre 88 y 112 mg/dl (percentil 40–80). Se observaron hallazgos similares al comparar C-LDL con ApoB.
La concordancia/discordancia puede definirse de múltiples maneras: discordancia por puntos de corte, discordancia por percentiles o discordancia por residuales.31 Independientemente del método, la concordancia y la discordancia representan diferentes proporciones entre los parámetros comparados. La discordancia por puntos de corte parece ser el método más intuitivo y clínicamente aplicable; los resultados de estos análisis sugieren que niveles elevados de C-LDL, C-noHDL o ApoB en personas no tratadas con medicación hipolipemiante conllevan un mayor riesgo de enfermedad cardiovascular. En cambio, en personas que sí reciben tratamiento, los niveles elevados de C-noHDL y ApoB parecen indicar mejor el riesgo residual.
¿Cómo se comparan la ApoB, el C-noHDL y el C-LDL como marcadores de riesgo cardiovascular?
Aunque existe una alta correlación entre los niveles de ApoB, C-LDL y C-noHDL, diversas situaciones clínicas pueden generar discordancias entre estos valores y su capacidad predictiva del riesgo cardiovascular.30-31 En este contexto, es importante tener en cuenta lo siguiente:
1) mientras que la ApoB refleja el número de partículas aterogénicas, la medición de LDL-C y C-noHDL cuantifica la masa de colesterol; y
2) especialmente en la comparación con el C-LDL, que es el principal objetivo terapéutico para reducir el riesgo cardiovascular, su determinación en muchos casos surge de la estimación mediante fórmulas que, como sabemos, son imprecisas.
Desde una perspectiva fisiopatológica, podría plantearse que si cada partícula que contiene ApoB transportara una cantidad constante de colesterol, los distintos marcadores lipídicos (ApoB, C-LDL y C-noHDL) tendrían un valor predictivo similar.32-33 Sin embargo, la evidencia actual sugiere que existe una variabilidad considerable en el contenido de colesterol por partícula de ApoB. Esta variabilidad está determinada, principalmente, por los procesos de intercambio de lípidos entre las lipoproteínas, los cuales dependen de múltiples factores, como por ejemplo, la concentración de triglicéridos.34-35 Como resultado, condiciones como la hipertrigliceridemia, la obesidad y la resistencia a la insulina pueden generar discrepancias entre estas mediciones, lo que se traduce en un aumento en el número de partículas de LDL (mayor concentración de ApoB), pero con un contenido reducido de colesterol (menor concentración de C-LDL).35
Diversos estudios han analizado la capacidad predictiva diferencial de estos tres marcadores. Considerando diferentes cohortes y puntos de análisis, la evidencia respalda que la concentración de ApoB está más estrechamente asociada con el riesgo de enfermedad cardiovascular aterosclerótica que el C-LDL y el C-noHDL.32, 36-38 Sin embargo, los pacientes tratados con estatinas constituyen una población particular, ya que estas drogas reducen preferentemente el C-LDL, lo que genera divergencias en relación con los niveles de ApoB y C-noHDL.
Los resultados del Copenhagen General Population Study, que incluyó a sujetos tratados con estatinas, refuerzan esta conclusión.39
En casos de discordancia entre los valores de ApoB y C-LDL, el riesgo cardiovascular se mostró más consistentemente relacionado con los niveles de ApoB. Específicamente, los participantes con niveles de ApoB por encima de la mediana y C-LDL por debajo de la mediana presentaron un mayor riesgo de mortalidad por todas las causas. En contraste, aquellos con ApoB por debajo de la mediana y C-LDL por encima de la mediana evidenciaron un menor riesgo de mortalidad. Resultados similares se observaron al analizar la discordancia entre ApoB y C-noHDL. Según el último Consenso de Expertos de la National Lipid Association (NLA), cuando existe discordancia entre ApoB y C-LDL, entre ApoB y C-noHDL, o entre C-LDL y C-noHDL, la ApoB se considera el predictor más fiable del riesgo cardiovascular.40
¿Cuál es la utilidad diagnóstica de la ApoB en la práctica clínica habitual?
La ApoB es un biomarcador excelente para optimizar la estratificación del riesgo cardiovascular, especialmente en pacientes con niveles “normales” de C-LDL pero alto riesgo cardiovascular.40-41 Esta medición es particularmente útil, ya que permite evaluar de manera más precisa el riesgo de enfermedad cardiovascular en estos pacientes. La ApoB es equivalente a cuantificar el número de lipoproteínas aterogénicas, ya que cada partícula contiene una única molécula de ApoB, lo que contribuye a una determinación más exacta del riesgo aterogénico.42-43
Dado que cada partícula de LDL contiene una cantidad específica de ApoB, en situaciones donde los valores de C-LDL son similares pero las concentraciones de ApoB varían, el tamaño y la densidad de las partículas de LDL pueden ser diferentes. Esto tiene implicaciones directas sobre la aterogenicidad de las partículas, lo que hace que la medición de ApoB sea especialmente útil cuando el C-LDL es bajo o se encuentra “controlado”, condiciones en las cuales el riesgo puede estar subestimado. Además, en pacientes con múltiples factores de riesgo, como hipertrigliceridemia, diabetes, obesidad abdominal, resistencia a la insulina o síndrome metabólico, es común encontrar partículas de LDL pequeñas y densas, las cuales están asociadas con un mayor riesgo de aterosclerosis prematura o acelerada.44 Por ello, en estos pacientes, la medición de ApoB proporciona información adicional y valiosa para la estratificación del riesgo cardiovascular. Asimismo, la medición de ApoB resulta útil para diferenciar entre la hipertrigliceridemia familiar y la hiperlipemia familiar combinada, dado que en la primera el valor de ApoB es normal, mientras que en la segunda se encuentra elevado.45-46
En resumen, la ApoB es un indicador específico y útil, que actúa como una herramienta complementaria a la medición de C-LDL. Su medición permite una evaluación personalizada del riesgo cardiovascular asociada a los lípidos y facilita el establecimiento de objetivos terapéuticos más precisos, lo que optimiza las estrategias para reducir la enfermedad cardiovascular aterosclerótica.
¿Cuáles son las situaciones en las que la medición de ApoB es especialmente útil?
a) Optimizar la estratificación del riesgo cardiovascular, particularmente en pacientes de alto o muy alto riesgo que presentan valores “normales” o “controlados” de C-LDL, según las metas terapéuticas establecidas. En estos casos, la presencia de ApoB elevada sugiere un mayor riesgo residual aterogénico y puede justificar la intensificación de las medidas terapéuticas.
b) Mejorar la estratificación del riesgo en pacientes con hipertrigliceridemia, diabetes, obesidad, resistencia a la insulina o síndrome metabólico, donde la estimación del C-LDL por fórmula no es recomendada, a la vez que el valor de C-LDL medido puede enmascarar la presencia de partículas pequeñas y densas.
¿Cuál es el impacto de los principales fármacos hipolipemiantes sobre los niveles de ApoB?
Diversas terapias hipolipemiantes han demostrado ser eficaces en la reducción de ApoB, lo que contribuye a la disminución del riesgo cardiovascular.
Las estatinas inhiben la HMG-CoA reductasa, lo que reduce la síntesis de colesterol y aumenta la expresión de los receptores LDL. Las estatinas de alta intensidad pueden reducir los niveles de ApoB entre un 30% y un 50%.47
El ezetimibe inhibe la absorción intestinal de colesterol a través del transportador NPC1L1. Cuando se asocia con estatinas, proporciona una reducción adicional de aproximadamente un 20% en los niveles de ApoB.48
Los inhibidores de PCSK9 (alirocumab y evolocumab) aumentan el reciclaje de los receptores LDL y facilitan la depuración de partículas que contienen ApoB. Estas terapias logran reducciones de ApoB de entre el 45% y el 55%.19-20 De manera similar, inclisiran, un ARN interferente pequeño (siRNA, de sus siglas en inglés), inhibe la síntesis hepática de PCSK9. Se administra dos veces al año y produce reducciones sostenidas de ApoB de aproximadamente un 43%.49
El ácido bempedoico inhibe la ATP-citrato liasa, una enzima que actúa antes de la HMG-CoA reductasa. Ya sea solo o en combinación con ezetimibe, reduce los niveles de ApoB entre un 14% y un 19%.50
Evinacumab es un anticuerpo monoclonal que inhibe ANGPTL3, promoviendo la lipólisis y la depuración de lipoproteínas que contienen ApoB. En pacientes con hipercolesterolemia familiar homocigota (HFHo), se ha observado una reducción promedio del 40,8% en los niveles de ApoB.51 Por otro lado, lomitapida, un inhibidor de la MTP, impide el ensamblaje de lipoproteínas que contienen ApoB, logrando reducciones de entre 29 y 56%.52
Finalmente, obicetrapib, un inhibidor oral, selectivo y de nueva generación de la proteína transportadora de ésteres de colesterol (CETP), conocido por su efecto significativo sobre lipoproteínas aterogénicas más allá de incrementar los niveles de C-HDL, ha demostrado reducir los niveles de ApoB en un 26,5% en comparación con placebo, según un reciente metaanálisis.53
Un resumen del impacto de los distintos fármacos sobre los niveles de ApoB se presenta en la Tabla 1:
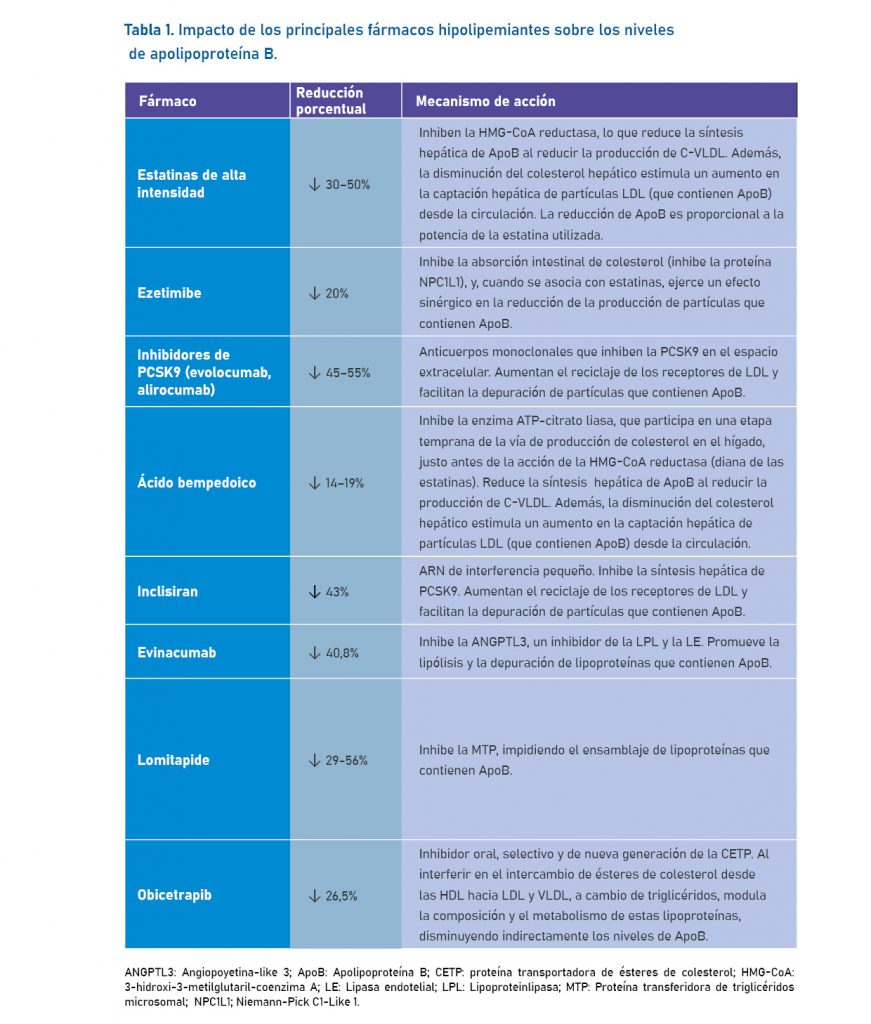
¿Cuáles son las metas actuales de ApoB?
Una de las primeras recomendaciones en favor del uso de ApoB en Estados Unidos (2009) provino de la Asociación Americana de Química Clínica, que respaldó la medición de ApoB como herramienta útil para la evaluación y el seguimiento de pacientes con riesgo de enfermedad cardiovascular.54
Las guías canadienses y europeas han recomendado la medición de ApoB en determinadas poblaciones desde hace varios años. Desde 2012, la guía de la Sociedad Cardiovascular Canadiense (CCS) para el diagnóstico y tratamiento de la dislipidemia reconoce el uso de la medición de ApoB en personas con niveles elevados de triglicéridos, definidos como >1,5 mmol/L (131 mg/dl).55 Asimismo, desde 2016, la Sociedad Europea de Cardiología (ESC) y la Sociedad Europea de Aterosclerosis (EAS) han recomendado considerar la medición de ApoB, cuando esté disponible, en pacientes con hipertrigliceridemia.56
La guía multisociedad de 2018 de la Asociación Americana del Corazón (AHA) y el Colegio Americano de Cardiología (ACC), elaborada en colaboración con diversas organizaciones médicas líderes, estableció que las personas con niveles de triglicéridos ≥ 200 mg/dl tienen una “indicación relativa” para la medición de ApoB.57 Además, la guía indica que un nivel de ApoB > 130 mg/dl debe considerarse un “factor potenciador de riesgo” a la hora de evaluar la necesidad de iniciar terapia hipolipemiante. Sin embargo, no se recomienda la realización de pruebas universales para ApoB en la población general.
En 2019, la ESC y la EAS recomendaron la medición de ApoB como una alternativa a la medición de C-LDL—e incluso, posiblemente, como preferida frente al C-noHDL— como marcador principal para la detección, diagnóstico y tratamiento en personas con triglicéridos elevados, diabetes, obesidad, síndrome metabólico o niveles muy bajos de C-LDL.58 La misma guía señaló que los niveles de C-LDL pueden subestimar el riesgo de enfermedad cardiovascular aterosclerótica, al no reflejar con precisión ni la concentración total de colesterol transportado por las LDL ni la cantidad total de lipoproteínas que contienen ApoB. Por su parte, el documento definió objetivos lipídicos secundarios para ApoB de <65 mg/dl, <80 mg/dl y <100 mg/dl en pacientes de riesgo muy alto, alto y moderadamente alto, respectivamente. Estos se corresponden con objetivos de C-LDL de <55 mg/dl, <70 mg/dl y <100 mg/dl. La guía de 2020 de la Asociación Americana de Endocrinólogos Clínicos (AACE) y el Colegio Americano de Endocrinología (ACE) destacó que la medición de ApoB puede ofrecer una evaluación más precisa de la aterogenicidad.59 La guía también reconoció el valor de ApoB en la evaluación de la eficacia del tratamiento hipolipemiante, ya que los niveles de ApoB pueden permanecer por encima del objetivo incluso después de alcanzar los valores objetivo de C-LDL. En su guía más reciente de 2021, la CCS recomendó el uso de ApoB o C-noHDL, en lugar de C-LDL, como medición lipídica preferida para el cribado en pacientes con triglicéridos >1,5 mmol/l (133 mg/dl).60 La CCS también sugirió un umbral de ApoB ≥70 mg/dl como criterio para intensificar el tratamiento hipolipemiante en pacientes con enfermedad cardiovascular aterosclerótica establecida. La declaración científica reciente de la NLA respaldó la medición de ApoB como una estrategia razonable, no solo para la evaluación lipídica inicial, sino también en pacientes que se encuentran bajo tratamiento hipolipemiante.60 Según este documento, los umbrales para iniciar o intensificar la farmacoterapia para los niveles de ApoB no están tan bien establecidos como para los niveles de C-LDL y C-noHDL. Sin embargo, basados en estudios poblacionales y en ensayos controlados aleatorizados de individuos tratados con hipolipemiantes, se sugiere que los umbrales de ApoB para pacientes con riesgo cardiovascular muy alto, alto o intermedio sean de 60, 70 y 90 mg/dl, respectivamente, para corresponderse con los umbrales de tratamiento actuales para C-LDL y C-noHDL. Un estudio realizado en Argentina demostró que, en una población sana, el percentilo 20 de ApoB fue de 72 mg/dl.61 Es relevante señalar que este valor se encuentra entre las metas de ApoB recomendadas por las guías ESC/EAS y NLA para personas con alto riesgo cardiovascular. Más aún, el percentilo 10 fue menor a 60 mg/dl, nivel coincidente con los objetivos lipídicos dados por las mismas recomendaciones para la población de muy alto riesgo. En contraste, un valor de ApoB superior a 117 mg/dl se observó en el 20% de los individuos con mayor concentración de partículas aterogénicas, lo que podría marcar un umbral de mayor riesgo vascular, incluso en personas aparentemente sanas.61
¿Qué debemos conocer sobre la hipobetalipoproteinemia?
La hipobetalipoproteinemia familiar (FHBL) se caracteriza por una concentración plasmática reducida de C-LDL por debajo del quinto percentilo para sexo y edad.62 Más frecuentemente la forma monogénica en adultos resulta de variantes heterocigotas de pérdida de función de la ApoB y menos frecuentemente de la PCSK9 llevando a un trastorno autosómico dominante. Las mutaciones en el gen de la ApoB resultan en la producción de proteínas ApoB truncadas (tanto de ApoB100 como de ApoB48) que afectan la capacidad hepática para exportar lipoproteínas, lo que provoca una acumulación de triglicéridos en los hepatocitos, aumentando el riesgo de desarrollar enfermedades hepáticas.63 La mutación en el ApoB48 afecta la absorción de lípidos desde el intestino, lo que conlleva malabsorción de grasas y vitaminas liposolubles, y se asocia con complicaciones gastrointestinales, neuromusculares, oftalmológicas y hematológicas. La forma homocigota o heterocigota compuesta (HoFHBL1) es rara y puede causar complicaciones graves y manifestaciones fenotípicas similares a la abetalipoproteinemia (ABL), un trastorno autosómico recesivo causado por mutaciones en la proteína de transferencia microsomal (MTP). La forma heterocigota (HeFHBL1) es relativamente común y, por lo general, asintomática, excepto por hipolipemia moderada y una tendencia a la esteatosis hepática.62
En un estudio reciente sobre FHBL, se identificaron más de 140 variantes del gen APOB.62 La frecuencia de ApoB truncada en la población general es de 1:3000 (HeFHBL1), mientras que la forma homocigota o heterocigota compuesta (HoFHBL1) tiene una incidencia estimada de menos de 1:1.000.000. La FHBL también puede ser causada por mutaciones en el gen de la angiopoyetina-like protein 3 (ANGPTL3), denominándose en este último caso FHBL2.
La HeFHBL1 suele ser asintomática, excepto por niveles bajos de C-LDL y de ApoB, que alcanzan aproximadamente un tercio de los niveles normales. Los pacientes pueden presentar disfunción hepática moderada, y el 5-10% desarrollan esteatosis hepática grave, con posibles complicaciones como cirrosis y cáncer hepático. Algunos casos raros presentan complicaciones neurológicas, posiblemente debido a deficiencia de vitaminas E y A. Por el contrario, los pacientes con HoFHBL1 tienen formas clínicas graves y presentan características fenotípicas similares a la ABL. Entre ellas se encuentra los trastornos neuromusculares (por déficit de vitamina E), trastornos oftalmológicos (por déficit de vitamina A), trastornos gastrointestinales (esteatorrea, déficit de crecimiento por síndrome de malabsorción, esteatosis hepática que rara vez progresa a cirrosis y hepatocarcinoma), anomalías en el metabolismo óseo (por déficit de vitamina D) y anomalías hematológicas.
El diagnóstico de FHBL1 se basa en la identificación de mutaciones genéticas, niveles extremadamente bajos de C-LDL y ApoB (menores de 15 mg/dl), y la presencia de síntomas clínicos. Se deben considerar diagnósticos diferenciales como la hipobetalipoproteinemia secundaria a enfermedades crónicas o terminales como cáncer, enfermedad hepática, hipertiroidismo, malabsorción de grasas por pancreatitis crónica y malnutrición.62
Recientemente, se han descrito formas poligénicas de hipobetalipoproteinemia asociadas con un menor riesgo de lesiones hepáticas y esteatosis en comparación con las formas monogénicas, que se diagnostican mediante un puntaje de riesgo poligénico y son más prevalentes en la población general que las mutaciones monogénicas previamente descritas.64
No existe un tratamiento específico para la FHBL. Este se enfoca en la suplementación con altas dosis de vitaminas liposolubles y ácidos grasos esenciales, con el fin de prevenir o retrasar las complicaciones. Además, es importante garantizar una ingesta calórica adecuada y restringir la ingesta de grasas para evitar retrasos en el crecimiento.
Finalmente, estos síndromes de colesterol bajo se han asociado con un menor riesgo de desarrollar enfermedades cardiovasculares, lo que ha abierto la puerta a nuevas estrategias terapéuticas. Un ejemplo de ello es el Mipomersen, un oligonucleótido antisentido (ASO) que inhibe la producción de ApoB100 y que se utiliza en pacientes con HFHo. Otro tratamiento relevante es el Lomitapide, que inhibe la producción de MTP y se emplea tanto en el tratamiento de la HFHo como en la quilomicronemia familiar (FCS).65
Conclusiones del documento
La ApoB se ha consolidado como un marcador lipídico clave en el manejo del paciente dislipidémico, aportando información diagnóstica y pronóstica de gran valor clínico. Al reflejar de manera directa la cantidad de partículas aterogénicas circulantes, su cuantificación permite estimar con mayor precisión el potencial aterogénico total. Esto se evidencia en la excelente correlación entre ApoB y C-LDL, aunque con una concordancia moderada entre ambos parámetros. Diversas evidencias epidemiológicas, genéticas y provenientes de estudios clínicos respaldan su valor pronóstico en la prevención de la enfermedad cardiovascular aterosclerótica. Asimismo, se cuenta con herramientas farmacológicas eficaces para reducir sus niveles. La incorporación rutinaria de ApoB en la evaluación del riesgo cardiovascular podría optimizar la estratificación y el abordaje terapéutico, especialmente en escenarios donde las concentraciones de C-LDL pueden subestimar el riesgo residual. En este contexto, el reconocimiento y la utilización de ApoB como objetivo terapéutico emergente podrían contribuir a disminuir de manera más efectiva la carga global de enfermedad cardiovascular.
Bibliografía
- Morze J, Melloni GEM, Wittenbecher C, Ala-Korpela M, Rynkiewicz A, et al. ApoB-containing lipoproteins: count, type, size, and risk of coronary artery disease. Eur Heart J. Apr 28:ehaf207, 2025.
- Mehta A, Shapiro MD. Apolipoproteins in vascular biology and atherosclerotic disease. Nat Rev Cardiol. 19(3):168-179, 2022.
- Dance GSC, Sowden MP, Cartegni L, Cooper E, Krainer AR, Smith HC. Two Proteins Essential for Apolipoprotein B mRNA Editing Are Expressed from a Single Gene through Alternative Splicing. J Biol Chem. 277(15):12703-12709, 2002.
- Devaraj S, Semaan JR, Jialal I. Bioquímica, Apolipoproteína B. Disponible en: https://www-ncbi-nlm-nih-gov.translate.goog/books/NBK538139/?_x_tr_sl=en&_x_tr_tl=es&_x_tr_hl=es&_x_tr_pto=sge
- Haas ME, Attie AD, Biddinger SB. The regulation of ApoB metabolism by insulin. Trends Endocrinol Metab. 24(8):391-397, 2013.
- Taghibiglou C, Carpentier A, Van Iderstine SC, Chen B, Rudy D, Aiton A, et al. Mechanisms of hepatic very low density lipoprotein overproduction in insulin resistance. Evidence for enhanced lipoprotein assembly, reduced intracellular ApoB degradation, and increased microsomal triglyceride transfer protein in a fructose-fed hamster model. J Biol Chem. 2000 Mar 24;275(12):8416-25.
- Contois JH, Langlois MR, Cobbaert C, Sniderman AD. Standardization of Apolipoprotein B, LDL-Cholesterol, and Non-HDL-Cholesterol. J Am Heart Assoc. 12(15):e030405, 2023.
- Warnick GR, Kimberly MM, Waymack PP, Leary ET, Myers GL. Standardization of measurements for cholesterol, triglycerides, and major lipoproteins. Lab Med. 39:48-90, 2008.
- Garcia E, Bennett DW, Connelly MA, Jeyarajah EJ, Warf FC, Shalaurova I, et al. The extended lipid panel assay: a clinically deployed high-throughput nuclear magnetic resonance method for the simultaneous measurement of lipids and Apolipoprotein B. Lipids Health Dis. 19(1):247, 2020.
- Langlois MR, Nordestgaard BG, Langsted A, Chapman MJ, Aakre KM, Baum H, et al. European Atherosclerosis Society (EAS) and the European Federation of Clinical Chemistry and Laboratory Medicine (EFLM) Joint Consensus Initiative. Quantifying atherogenic lipoproteins for lipid-lowering strategies: consensus-based recommendations from EAS and EFLM. Clin Chem Lab Med. 58(4):496-517, 2020.
- Johannesen CDL, Langsted A, Nordestgaard BG, Mortensen M. Excess Apolipoprotein B and Cardiovascular Risk in Women and Men. J Am Coll Cardiol. 83(23):2262-2273, 2024.
- Sniderman AD, Williams K, Contois JH, Moroe HM, McQueen MJ, de Graaf J, et al. A meta-analysis of low-density lipoprotein cholesterol, non-high-density lipoprotein cholesterol, and apolipoprotein B as markers of cardiovascular risk. Circ Cardiovasc Qual Outcomes. 4(3):337-345, 2011.
- Richardson TG, Sanderson E, Palmer TM, Ala-Korpela M, Ference BA, Davey Smith G, et al. Evaluating the relationship between circulating lipoprotein lipids and apolipoproteins with risk of coronary heart disease: A multivariable Mendelian randomisation analysis. PLoS Med. 17(3):e1003062, 2020.
- Ference BA, Kastelein JJP, Ginsberg HN, Chapman MJ, Nicholls SJ, Ray KK, et al. Association of genetic variants related to CETP inhibitors and statins with lipoprotein levels and cardiovascular risk. JAMA. 318(10):947-956, 2017.
- Gotto AM, Whitney E, Stein EA, Shapiro DR, Clearfield M, Weis S, et al. Relation between baseline and on-treatment lipid parameters and first acute major coronary events in the Air force/Texas Coronary Atherosclerosis Prevention Study (AFCAPS/TexCAPS). Circulation. 101:477-484, 2000.
- Pedersen TR, Olsson AG, Faergeman O, Kjekshus J, Wedel H, Berg K, et al. Lipoprotein changes and reduction in the incidence of major coronary heart disease events in the Scandinavian Simvastatin Survival Study (4S). Circulation. 97:1453-60, 1998.
- Thanassoulis G, Williams K, Ye K; Brook R, Couture P, Patrick R, Lawler PR, et al. Relations of Change in Plasma Levels of LDL-C, Non-HDL-C and apoB With Risk Reduction From Statin Therapy: A Meta-Analysis of Randomized Trials. J Am Heart Assoc. 3(2):e000759, 2014.
- Cannon CP, Blazing MA, Giugliano RP, McCagg A, White JA., Theroux P, et al. Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes. N Engl J Med 372(25):2387–2397, 2015.
- Sabatine MS, Giugliano RP, Keech AC, Honarpour N, Wiviott SD, Murphy SA, et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. N Engl J Med. 376:1713-1722, 2017.
- Schwartz GG, Steg PG, Szarek M, Bhatt DL, Bittner VA, Diaz R, et al. Alirocumab after Acute Coronary Syndrome. N Engl J Med. 379(22):2097-2107, 2018.
- Hopewell JC, Chen F, Wallendszus K, Stevens W, Collins R, Wiviott SD, et al. Effects of Anacetrapib in Patients with Atherosclerotic Vascular Disease. N Engl J Med. 377(13):1217-1227, 2017.
- Bhatt D, Steg P., Miller M, Brinton EA, Jacobson T, Ketchum SB, et al. Reduction of Cardiovascular Events with Icosapent Ethyl for Hypertriglyceridemia. N Engl J Med. 380(1):11-22, 2019.
- Nicholls SJ, Lincoff M, García M, Bash D, Ballantyne CM, Barter PJ, et al. Effect of High-Dose Omega-3 Fatty Acids vs Corn Oil on Major Adverse Cardiovascular Events in Patients at High Cardiovascular Risk: The STRENGTH Randomized Clinical Trial. JAMA 324(22):2268-2280, 2020.
- Khan SU, Khan MU, Valavoor S, Khan MS, Okunrintemi V, Mamas MA, et al. Lipid-Lowering Therapies and Clinical Outcomes. Eur J Prev Cardiol. 27(12):1255-1268, 2020.
- Ference BA, Cannon CP, Landmesser U, Lüscher TF, Catapano AL, Ray KK, et al. Reduction of LDL and Cardiovascular Outcomes. Eur Heart J. 39:2540-2545, 2018.
- Liu J, Tang W, Chen G, Lu Y, Feng C, Tu XM. Correlation and agreement: overview and clarification of competing concepts and measures. Shanghai Arch Psychiatry. 28(2):115-120, 2016.
- Pencina KM, Pencina MJ, Lawler PR, Engert JC, Dufresne L, Ridker PM, et al. Interplay of Atherogenic Particle Number and Particle Size and the Risk of Coronary Heart Disease. Clin Chem. 69(1):48-55, 2023
- Cantey EP, Wilkins JT. Discordance between lipoprotein particle number and cholesterol content: an update. Curr Opin Endocrinol Diabetes Obes. 25(2):130–136, 2018.
- Idris I, Tate H, Ahmad A, McCormack T. Concordance between plasma apolipoprotein B levels and cholesterol indices among patients receiving statins and nonstatin treatment: Post-hoc analyses from the U.K. InPractice study. J Clin Lipidol. 5(4):316-23, 2011.
- Sniderman AD, Dufresne L, Pencina KM, Bilgic S, Thanassoulis G, Pencina MJ. Discordance among apoB, non-high-density lipoprotein cholesterol, and triglycerides: implications for cardiovascular prevention. Eur Heart J. 45(27):2410-2418, 2024.
- Johannesen CDL, Mortensen MB, Børge Nordestgaard BG, Langsted A. Discordance analyses comparing LDL cholesterol, Non-HDL cholesterol, and apolipoprotein B for cardiovascular risk estimation. Atherosclerosis. 403:119139, 2025.
- Wilkins JT, Li RC, Sniderman A, Chan C, DM Lloyd-Jones. Discordance between apolipoprotein B and LDL-cholesterol in young adults predicts coronary artery calcification: the CARDIA study. J Am Coll Cardiol. 67(2):193-201, 2016.
- Glavinovic T, Thanassoulis G, de Graaf J, Couture P, Hegele RA, Sniderman AD. Physiological Bases for the Superiority of Apolipoprotein B Over Low-Density Lipoprotein Cholesterol and Non-High-Density Lipoprotein Cholesterol as a Marker of Cardiovascular Risk. J Am Heart Assoc. 11(20):e025858, 2022.
- Nurmohamed NS, Ditmarsch M, Kastelein JJP. Cholesteryl ester transfer protein inhibitors: from high-density lipoprotein cholesterol to low-density lipoprotein cholesterol lowering agents? Cardiovasc Res. 118(14):2919-2931, 2022.
- Griffin BA, Freeman DJ, Tait GW, Thomson J, Caslake MJ, Packard CJ, et al. Role of plasma triglyceride in the regulation of plasma low density lipoprotein (LDL) subfractions: relative contribution of small, dense LDL to coronary heart disease risk. Atherosclerosis. 106:241–253, 1994.
- Sniderman AD, Islam S, Yusuf S, McQueen MJ. Discordance analysis of apolipoprotein B and non-high density lipoprotein choles-terol as markers of cardiovascular risk in the INTERHEART study. Atherosclerosis. 225(2):444–449, 2012.
- Cromwell WC, Otvos JD, Keyes MJ, Pencina MJ, Sullivan L, Vasan RS, et al. LDL particle number and risk of future cardiovascular disease in the Framingham offspring study - implications for LDL management. J Clin Lipidol. 1(6):583-592, 2007.
- Pencina MJ, D’Agostino RB, Zdrojewski T, Williams K, Thanassoulis G, Furberg CD, et al. Apolipoprotein B improves risk assessment of future coronary heart disease in the Framingham heart study beyond LDL-C and non-HDL-C. Eur J Prev Cardiol. 22(10):1321-1327, 2015.
- Johannesen CDL, Langsted A, Mortensen MB, Nordestgaard BG. Apolipoprotein B and non-HDL cholesterol better reflect residual risk than LDL cholesterol in statin-treated patients in the Copenhagen General Population Study. Eur Heart J. 42(5):474-482, 2021.
- Soffer D, Marston NA, Maki K, Jacobson T, Bittner V, Peña JM, et al. Role of apolipoprotein B in the clinical management of cardiovascular risk in adults: An Expert Clinical Consensus from the National Lipid Association. J Clin Lipidol.18(5):e647-e663, 2024.
- Ahmad M, Sniderman AD, Hegele RA. Apolipoprotein B in cardiovascular risk assessment. CMAJ. 195:E1124, 2023.
- Iavinovic T, Thanassoulis G, de Graaf J. Physiological bases for the superiority of apolipoprotein B over low-density lipoprotein cholesterol and non-high-density lipoprotein cholesterol as a marker of cardiovascular risk. J Am Heart Assoc. 11:e025858, 2022.
- Cole J, Otvos DJ, Remaley TA. A Translational Tool to Facilitate Use of Apolipoprotein B for Clinical Decision-Making. Clinical Chemistry. 69(1):41-47, 2023.
- Alpert J, Stone NJ. The Importance of Apo B and Lipoprotein Little a [Lp(a)]. Am J Med. 137(12):1149-1150, 2024.
- Díaz JA, Castro-Cabezas M, Liemc A. Utilidad de la medición de la apolipoproteína B en la práctica clínica. Clin Invest Arterioscl. 17(3):142-146. 2005.
- Pedro-Botet J, Climent E, Gabarró N, Millán J. Hiperlipemia familiar combinada/hiperlipemia mixta poligénica. Clin Invest Arterioscler. 33:43-49, 2021.
- Baigent C, Blackwell L, Emberson J, Holland LE, Reith C, Bhala N. Efficacy and safety of cholesterol-lowering treatment: prospective meta-analysis of data from 90,056 participants in 14 randomised trials of statins Lancet. 366(9493):1267-1278. 2005.
- Tremblay AJ, Lamarche B, Hogue JC, Couture P. Effects of ezetimibe and simvastatin on apolipoprotein B metabolism in males with mixed hyperlipidemia. J Lipid Res. 50(7):1463-1471, 2009.
- Ray KK, Wright RS, Kallend D, Koenig W, Leiter LA, Raal FJ. Two Phase 3 Trials of Inclisiran in Patients with Elevated LDL Cholesterol. N Engl J Med. 382(16):1507-1519, 2020.
- Goldberg AC, Leiter LA, Stroes ESG, Baum SJ, Hanselman JC, Bloedon LT, et al. Effect of Bempedoic Acid vs Placebo Added to Maximally Tolerated Statins on Low-Density Lipoprotein Cholesterol in Patients at High Risk for Cardiovascular Disease: The CLEAR Wisdom Randomized Clinical Trial. JAMA. 322(18):1780-1788, 2019.
- Koseki M, Stroes E, Ali S, Banerjee P, Chan KC, Khilla N, et al. The Long-Term Efficacy and Safety of Evinacumab in Patients With Homozygous Familial Hypercholesterolemia. JACC Adv. 2(9):100648, 2023.
- Cuchel M, Meagher EA, du Toit Theron H, Blom DJ, Marais AD, Hegele RA, et al. Efficacy and safety of a microsomal triglyceride transfer protein inhibitor in patients with homozygous familial hypercholesterolaemia: a single-arm, open-label, phase 3 study. N Engl J Med. 368(2):1277-1287. 2013.
- Masson W, Barbagelata L, Lobo M, Nogueira JP, Handelsman Y. Lipid-lowering efficacy of obicetrapib: A comprehensive systematic review and meta-analysis. J Clin Lipidol. Dec 30:S1933-2874(24)00301-5, 2024.
- Contois JH, McConnell JP, Sethi AA, Csako G, Devaraj S, Hoefner DM, et al. Apolipoprotein B and cardiovascular


